Crohns sykdom er en kronisk inflammatorisk tarmsykdom. Behandlingen er primært medisinsk. Flere medikamenter er aktuelle ved behandling; lokale og systemiske steroider, thiopurin, metotreksat, biologisk behandling og anti-intergrin og anti-interleukin. Årsaken til Crohns sykdom er ikke kjent, og kurativ behandling er derfor ikke tilgjengelig. Omkring halvparten av pasientene vil være i behov av kirurgi i løpet av ti år etter at diagnosen er stilt (1).
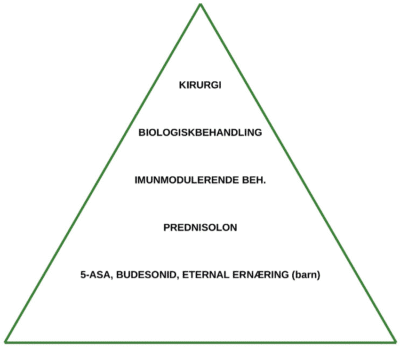
Figur 1. Behandlingspyramiden ved inflammatorisk tarmsykdom. (Tegnet av Stian Wendelborg og Trond Dehli)
Behandlingen har tradisjonelt fulgt en gradvis opptrapping (Figur 1). Avhengig av effekt og alvorlighetsgrad av sykdommen, kan man bevege seg opp og ned i behandlingspyramiden (2). Andre har argumentert for en «top-down» tilnærming, med fokus på nedtrapping av behandling når man har oppnådd behandlingsmålsettingen.
Kirurgi har tradisjonelt fremstått som siste alternativ når medisinsk behandling ikke har effekt. Denne tilnærmingen til kirurgisk behandling er utfordret av særlig LIR!C-studien (3). LIR!C-studien er en randomisert studie som sammenligner laparoskopisk ileocoecal reseksjon og biologisk behandling (Infliximab) hos voksne pasienter med Mb Crohn med begrenset ikke-stenoserende ileocoecal affeksjon (< 40 cm) og med utilstrekkelig effekt av immunmodulerende behandling. Studien viser at kirurgi er et godt behandlingsalternativ hos pasienter med terminal ileitt der konvensjonell behandling ikke er tilstrekkelig. Det ble ikke funnen noen forskjell i livskvalitet mellom gruppene etter 12 måneder, som var studiens primære endepunkt. Etter mer enn fem år klarte 42 % av pasientene i kirurgi-gruppen seg uten medikamentell behandling og ingen av pasientene trengte ytterligere reseksjoner (4). I Infliximab-gruppen gjennomgikk nærmere halvparten av pasientene en Crohns-relatert reseksjon.
Indikasjoner for kirurgi
De vanligste indikasjonene for kirurgi ved Crohns sykdom er symptomgivende stenose, fistler/abscess og behandlingsresistent sykdom. Mer sjeldne indikasjoner er blødning, påvirket vekst hos barn og utvikling av kreft.
Kirurgisk tilgang
Laparoskopisk kirurgi foretrekkes fremfor åpen kirurgi ved inflammatorisk tarmsykdom dersom det er mulig. IBD-pasienter har samme fordeler av mini-invasiv teknikk som andre pasienter (1).
Timing av kirurgi
Elektiv kirurgi gir mindre komplikasjoner, mindre konverteringer fra laparoskopisk kirurgi til åpen kirurgi og færre stomier enn ved akutt kirurgi (1,5). Så fremt det er mulig, bør pasientene optimaliseres før kirurgi med tanke på ernæring, justering av medikamenter, røykestopp og kontroll på sepsis/abscesser/fistler. LIR!C-studien har vist at tidlig kirurgi ved ileocoecal sykdom, altså før man starter biologisk behandling, kan være fordelaktig (3). Ved fistulerende sykdom, kan det også være en fordel med kirurgi tidlig, før sykdommen blir mer komplisert med behov for større kirurgi.
Abscesser og fistler
Intra-abdominale abscesser bør behandles med antibiotika og dreneres perkutant, hvis det ligger til rette for det. Abscessdrenasje gir bedre infeksjonskontroll og er i noen tilfeller tilstrekkelig behandling. Vanligvis utføres abscessdrenasje ultralyd- eller CT-veiledet. Hvis abscessen ikke går tilbake, eller ved allerede etablert fistel, kan det bli nødvendig med kirurgi og da oftest med reseksjon av det affiserte tarmavsnittet. Perkutan drenasje i forkant er likevel en fordel for å oppnå bedre kontroll med infeksjonen og eventuell sepsis (1).
Fistler mellom forskjellige tarmavsnitt og fistler til hud med liten produksjon er ikke alene indikasjon for kirurgi (1).
Strikturer
Ved etablerte strikturer er det kliniske bildet variabelt, fra milde, takvise magesmerter til ileus.
Inflammatoriske stenoser skal behandles medisinsk, mens etablerte, fibrøse stenoser må opereres. Radiologisk vurdering (MR) kan til en viss grad skille mellom disse. Ved kortere stenoser (<5 cm) som kan nås endoskopisk, kan ballongdilatasjon vurderes.
Ved operasjon er det vanligst å resesere det syke tarmavsnittet til frisk tarm på begge sider før man anlegger en anastomose. Man anbefaler 2 cm fri reseksjonsrand (makroskopisk). Hvis det er flere stenoser eller pasienten har gjennomgått tarmreseksjon(er) tidligere, er det mer aktuelt å gjøre strikturplastikker for å unngå kort-tarm og ernæringsproblemer. De to vanligste strikturplastikkene er å åpne stenosen på langs og lukke på tvers for de korte (Heinecke-Mikulicz) og side-til-side anastomose for de lange (Finney)(Figur 2) (6).
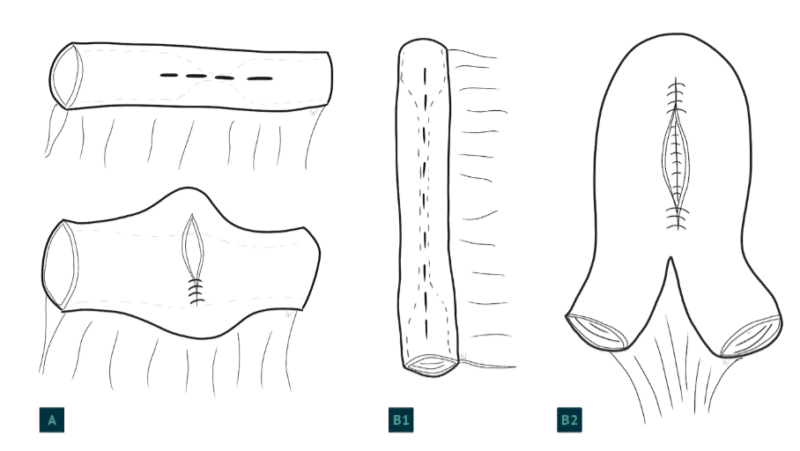
Figur 2. Strikturplastikker. A) Plastikk ved korte stenoser, Heinecke-Mikulicz. B1 og B2) Plastikk ved lengre stenoser, Finney.
Studier har vist gode resultater ved strikturplastikk, også over tid (7,8). Det er vanskelig å sammenligne strikturplastikk og reseksjon med anastomose, da studiene og meta-analysene bygger på ikke-randomiserte data (7–9). Strikturplastikk har sannsynligvis residivrate omtrent som ved reseksjon.
Anastomoseteknikk/Kono-S
Kirurgisk teknikk ved anleggelse av anastomose har vært undersøkt i mange studier. I hovedsak har man sammenlignet ende-til-ende og sidetil-side (Figur 3), hvor både stapler og manuell sutur er brukt. Det er gjort flere meta-analyser som baserer seg på en del svake kohortstudier og delvis gamle data, hvor man likevel finner noe støtte for at side-til-side-anastomose bidrar til færre postoperative komplikasjoner, færre klinisk residiv og færre reoperasjoner (10,11). I europeiske retningslinjer anbefales det side-side-anastomose ved ileocolisk reseksjon og tynntarmreseksjon hos pasienter med Mb Crohns (1).
Kono-S er en anastomoseteknikk som isolerer selve anastomosen fra kontakt med mesenteriet (Figur 4) (12). En fersk meta-analyse basert på 15 studier og 1500 pasienter tyder på at Kono-S anastomose kommer bedre ut enn konvensjonell anastomose når det gjelder residiv vurdert endoskopisk (41 % for Kono-S, 48 % for tarmreseksjon), residiv med behov for ytterligere kirurgi (2,7 % for Kono-S, 21 % for tarmreseksjon), samt risiko for anastomoselekkasje (1,7 % for Kono-S, 4,9 % for tarmreseksjon) (13). Dette resultatet er bekreftet i en randomisert studie (14). En annen randomisert studie har ikke funnet noen forskjell mellom konvensjonell anastomose og Kono-S (15). Europeiske retningslinjer åpner for å benytte Kono-S-anastomosen ved andre reseksjoner enn ileocoecal reseksjon (1). Det skal nevnes at en vanlig antimesenteriell side-til-side anastomose (Figur 3) også vil isolere selve anastomosen fra mesenteriet slik som Kono-S, men dette er lite problematisert i studiene nevnt her.
Crohn i Kolon og rektum
Ved Crohn-affeksjon av kolon og rektum blir beslutninger og kirurgisk behandlingsvalg mer komplekse. Indikasjonene for reseksjon av et eller flere kolonsegmenter er stenoser og fistler, samt symptomgivende inflammasjon på tross av medisinsk behandling.
Hvis et begrenset segment av kolon er affisert, er segmental kolonreseksjon et alternativ (1). Ved to affiserte segmenter eller mer omfattende affeksjon, er kolektomi anbefalt (1).
Hos pasienter med Crohn-affeksjon i kolon, rektum og/eller analt kan det være situasjoner hvor anleggelse av avlastende stomi er indisert. Hvis man anlegger stomi oralt for Crohn-affisert tarm, vil inflammasjonen som hovedregel falle til ro i tarmsegmentene distalt for stomien. Dette gjelder spesielt for rektal og anal Crohn.
Ved kolektomi, kan man enten anlegge en ileostomi eller ileorektal anastomose. Ileorektal anastomose kan være et godt valg, men det krever at pasienten har normal sfinkterfunksjon, rektal kapasitet omkring 150 ml målt ved oppfyllingstest (ballong i rektum som fylles med vann), og ikke har inflammasjon i rektum/analkanal. Ved gjenværende rektumstump og ved ileorektal anastomose, må man huske på økt risiko for utvikling av kreft, og rektum bør derfor kontrolleres jevnlig endoskopisk (16).
Mesenteriell reseksjon
Det er vanlig å fjerne den fortykkede delen av mesenteriet ved tynntarmreseksjon med som oftest en partiell reseksjon av mesenteriet i tilknytning til det syke tarmavsnittet som skal fjernes.
En kohortstudie fra Irland tyder på bedre effekt av mer radikal fjerning av mesenteriet (17). To studier har vist gode resultater med mer radikal reseksjon av mesenteriet, med mindre postoperativt residiv av Crohn (18,19). En randomisert studie med totalt 131 pasienter som fikk ileocoecal reseksjon ved seks sentre i Nederland og Italia, viste ingen endoskopisk forskjell med hensyn til Crohn residiv mellom utvidet mesenteriell reseksjon og mesenteriell-sparende kirurgi (19). En fersk systematisk oversikt og meta-analyse konkluderer med det samme (20).
Forebygging av residiv etter kirurgi
Til forskjell fra kirurgi ved ulcerøs kolitt, er ikke kirurgi ved Mb Crohn kurativ. Residiv kan forekomme allerede noen uker etter kirurgi, og det kan gå mange år til residivet kommer. Ofte involverer residivet den opererte delen av gastrointestinaltraktus, i særlig grad selve anastomoseområdet. Risikofaktorer for residiv inkluderer tidligere kirurgi, fistulerende sykdom og histologiske funn (granulomer, myenterisk pleksitt) (21). Disse kan vi ikke gjøre noe med.
Røyking gir både økt risiko for residiv og økt risiko for mer alvorlig sykdom enn for ikke-røykere ved Crohns sykdom (22).
Kirurgisk teknikk kan muligvis påvirke risikoen for residiv. Ved reseksjon av tarm er det ikke redusert residivrisiko med vide reseksjonsmarginer (12 cm) sammenlignet med kort reseksjonsmargin (2 cm) (23). Ved omhyggelig palpasjon av den mesenterielle randen kan man identifisere overgangen mellom inflammert og ikke-inflammert tarm (24). Ved valg av anastomosetype bør man ha i tankene, at mange pasienter vil bli tilbudt koloskopisk kontroll 6-12 måneder etter kirurgi. Her vurderes primært graden av inflammasjon i anastomoseområdet, og anti-peristaltiske side-til-side-anastomoser kan være vanskeligere å vurdere endoskopisk enn andre anastomosetyper. Det vil også være vanskeligere å utføre endoskopisk ballong-dilatasjon av en anti-peristaltisk anastomose. Anastomose bør likevel anlegges side-til-side (1). Både Kono-S-anastomosen og utvidet mesenteriell reseksjon vil kreve større, randomiserte studier for å få avklart bedre hvilken plass de bør ha i behandlingen.
Medisinsk behandling kan bidra til å redusere risikoen for residiv etter kirurgi. Det er flere strategier for medisinsk behandling for å redusere residivforekomsten. Man kan gi det til alle, man kan avvente til gjennomført endoskopi 6-12 måneder etter kirurgi, eller man kan stratifisere etter risikofaktorer som røyking, tidligere kirurgi, penetrerende sykdom, granulomer i resektatet, myenterisk pleksitt, <30 års alder ved operasjonstidspunktet, >50 cm tarmreseksjon og perianal sykdom. Det er ikke enighet om hvilke risikofaktorer man skal ta hensyn til, om grensen går ved en eller flere enn en risikofaktor, og det er ikke entydig hva profylaksen skal bestå av (21).
Metronidazol i lav dose (20 mg/kg/døgn) har i en randomisert studie redusert residiv signifikant sammenlignet med placebo (25). En Cochrane-analyse så på effekt av residiv etter kirurgi for Crohn ved flere medikamenter, og fant noe holdepunkt for at adalimumab kan redusere risikoen for residiv etter kirurgi sammenlignet med placebo (26). I Storbritannia anbefaler man azathioprin og metronidazol i tre måneder etter kirurgi, og man fraråder bruk av biologisk behandling som profylakse. Her tar man også hensyn til kostnader (27). Europeiske retningslinjer har først i 2024 fått et eget punkt om medisinsk profylakse til pasienter med høy risiko for residiv på grunn av røyking, penetrerende sykdom, intra-abdominal abscess og/eller fistel (1). Bruk av thiopuriner og biologisk behandling blir foreslått.
Ved UNN Tromsø har vi valgt å gi seks måneder med biologisk behandling og tre måneder med metronidazol som profylakse til alle pasienter uten gjenværende sykdom.
Referanser
1. Adamina M, Minozzi S, Warusavitarne J, Buskens CJ, Chaparro M, Verstockt B, et al. ECCO Guidelines on Therapeutics in Crohn's Disease: Surgical Treatment. J Crohn's Colitis. 2024;18(10):1556–82.
2. Buer LCT MB. Inflammatorisk tarmsykdom – diagnostikk og behandling. Indremedisineren [Internet]. 2016; Available from: https://indremedisineren.no/2016/08/inflammatorisk-tarmsykdom-diagnostikk-og-behandling/
3. Ponsioen CY, de Groof EJ, Eshuis EJ, Gardenbroek TJ, Bossuyt PMM, Hart A, et al. Laparoscopic ileocaecal resection versus infliximab for terminal ileitis in Crohn's disease: a randomised controlled, open-label, multicentre trial. Lancet Gastroenterol Hepatol [Internet]. 2017 Nov 1 [cited 2025 Aug 17];2(11):785–92. Available from: https://www.sciencedirect.com/science/article/abs/pii/S2468125317302480
4. Stevens TW, Haasnoot ML, D'Haens GR, Buskens CJ, de Groof EJ, Eshuis EJ, et al. Laparoscopic ileocaecal resection versus infliximab for terminal ileitis in Crohn's disease: retrospective long-term follow-up of the LIR!C trial. Lancet Gastroenterol Hepatol [Internet]. 2020 Oct 1 [cited 2025 Aug 17];5(10):900–7. Available from: https://www.sciencedirect.com/science/article/abs/pii/S2468125320301175?via%3Dihub
5. Udholm LS, Rasmussen SL, Madsbøll TK, Omairi M, El-Hussuna A. A systemic review and metaanalysis of postoperative outcomes in urgent and elective bowel resection in patients with Crohn's disease. Int J Colorectal Dis. 2021;36(2):253–63.
6. Roy P, Kumar D. Strictureplasty. Br J Surg. 2004;91(11):1428–37.
7. Uchino M, Ikeuchi H, Matsuoka H, Matsumoto T, Takesue Y, Tomita N. Long-term efficacy of strictureplasty for Crohn's disease. Surg Today. 2010;40(10):949–53.
8. Rottoli M, Tanzanu M, Manzo CA, Bacchi Reggiani ML, Gionchetti P, Rizzello F, et al. Strictureplasty for Crohn's disease of the small bowel in the biologic era: long-term outcomes and risk factors for recurrence. Tech Coloproctol [Internet]. 2020;24(7):711–20. Available from: https://doi.org/10.1007/s10151-020-02208-7
9. Butt WT, Ryan ÉJ, Boland MR, McCarthy EM, Omorogbe J, Hazel K, et al. Strictureplasty versus bowel resection for the surgical management of fibrostenotic Crohn's disease: a systematic review and meta-analysis. Int J Colorectal Dis. 2020;35(4):705–17.
10. Luglio G, Corcione F. Stapled versus handsewn methods for ileocolic anastomoses. Tech Coloproctol. 2019;23(11):1093–5.
11. Feng JS, Li JY, Yang Z, Chen XY, Mo JJ, Li SH. Stapled side-to-side anastomosis might be benefit in intestinal resection for Crohn's disease. Med (United States). 2018;97(15):1–6.
12. Dasharathy SS, Limketkai BN, Sauk JS. What's New in the Postoperative Management of Crohn's Disease? Dig Dis Sci [Internet]. 2022;67(8):3508–17. Available from: https://doi.org/10.1007/s10620-021-07205-w
13. Lin W, Lemke M, Ghuman A, Phang PT, Brown CJ, Raval MJ, et al. Effect of Kono-S anastomosis on reducing postoperative recurrence rates in Crohn's disease: a systematic review and meta-analysis. Tech Coloproctol [Internet]. 2024;28(1):1–11. Available from: https://doi.org/10.1007/s10151-024-02991-7
14. Luglio G, Rispo A, Imperatore N, Giglio MC, Amendola A, Tropeano FP, et al. Surgical Prevention of Anastomotic Recurrence by Excluding Mesentery in Crohn's Disease: The SuPREMe-CD Study – A Randomized Clinical Trial. Ann Surg. 2020;272(2):210–7.
15. Tyrode G, Lakkis Z, Vernerey D, Falcoz A, Clairet V, Alibert L, et al. KONO-S Anastomosis Is Not Superior to Conventional Anastomosis for the Reduction of Postoperative Endoscopic Recurrence in Crohn's Disease. Inflamm Bowel Dis. 2024;30(10):1670–7.
16. Stjärngrim J, Widman L, Schmidt PT, Ekbom A, Forsberg A. Post-endoscopy colorectal cancer after colectomy in inflammatory bowel disease patients: A population-based register study. Eur J Gastroenterol Hepatol. 2023;35(3):288–93.
17. Coffey CJ, Kiernan MG, Sahebally SM, Jarrar A, Burke JP, Kiely PA, et al. Inclusion of the mesentery in ileocolic resection for Crohn's disease is associated with reduced surgical recurrence. J Crohn's Colitis. 2018;12(10):1139–50.
18. Zhu Y, Qian W, Huang L, Xu Y, Guo Z, Cao L, et al. Role of Extended Mesenteric Excision in Postoperative Recurrence of Crohn's Colitis: A Single-Center Study. Clin Transl Gastroenterol. 2021;12(10):1–9.
19. van der Does de Willebois EML, Bellato V, Duijvestein M, van der Bilt JDW, van Dongen K, Spinelli A, et al. Effect of mesenteric sparing or extended resection in primary ileocolic resection for Crohn's disease on postoperative endoscopic recurrence (SPICY): an international, randomised controlled trial. Lancet Gastroenterol Hepatol [Internet]. 2024 Sep 1 [cited 2025 Aug 17];9(9):793–801. Available from: https://www.sciencedirect.com/science/article/abs/pii/S2468125324000979?via%3Dihub
20. Mostafa OES, Zaman S, Malik M, Kumar P, Kumar L, Akingboye A, et al. Clinical outcomes of conventional versus extended mesenteric resection in limited ileo-colonic Crohn's disease: a systematic review and meta-analysis. Int J Colorectal Dis [Internet]. 2025;40(1). Available from: https://doi.org/10.1007/s00384-025-04937-3
21. Spertino M, Gabbiadini R, Dal Buono A, Busacca A, Franchellucci G, Migliorisi G, et al. Management of Post-Operative Crohn's Disease: Knowns and Unknowns. J Clin Med. 2024;13(8).
22. Yamamoto T, Keighley MRB. Smoking and disease recurrence after operation for Crohn's disease. Br J Surg. 2000;87(4):398–404.
23. Ryan JM, Rogers AC, O'Toole A, Burke JP. Meta-analysis of Histological Margin Positivity in the Prediction of Recurrence after Crohn's Resection. Dis Colon Rectum. 2019;62(7):882.
24. Delaney CP, Fazio VW. Crohn ' S Disease of the. 2001;81(1):137–58.
25. Rutgeerts P, Hiele M, Geboes K, Peeters M, Penninckx F, Aerts R, et al. Controlled trial of metronidazole treatment for prevention of crohn's recurrence after ileal resection. Gastroenterology. 1995;108(6):1617–21.
26. Gordon M, Clegg A, Sc F, Jk M, Ak A, Gordon M, et al. Crohn ' s disease : a network meta-analysis ( Review ). 2019;
27. Crohn's disease: management [Internet]. National Institute for Health and Care Excellence; 2019. Available from: https://www.nice.org.uk/guidance/ng129







