Til tross for store fremskritt innen medikamentell behandling av ulcerøs kolitt (UC), er kirurgi fortsatt eneste behandlingsalternativ for pasienter med dårlig respons på medikamentell behandling, især ved akutt alvorlig UC og for pasienter med UC-relatert neoplasi. Kirurgi for UC innebærer nesten alltid kolektomi. Bekkenreservoar, der tarmkontinuiteten reetableres, er et av flere alternativer for disse pasientene. Andre alternativer er permanent ileostomi, mer sjeldent kontinent ileostomi (Kocks reservoar) og ileorektal anastomose.
Litt historie
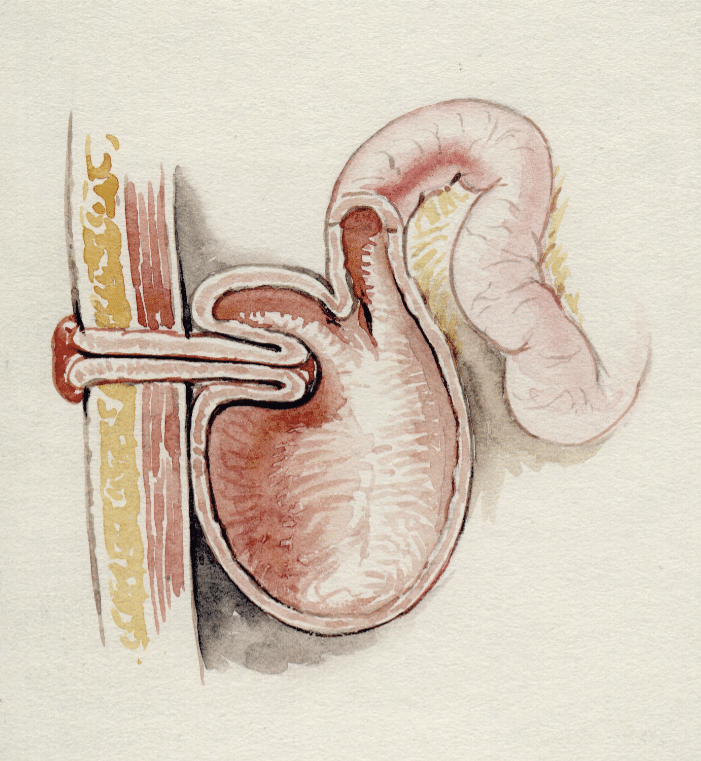
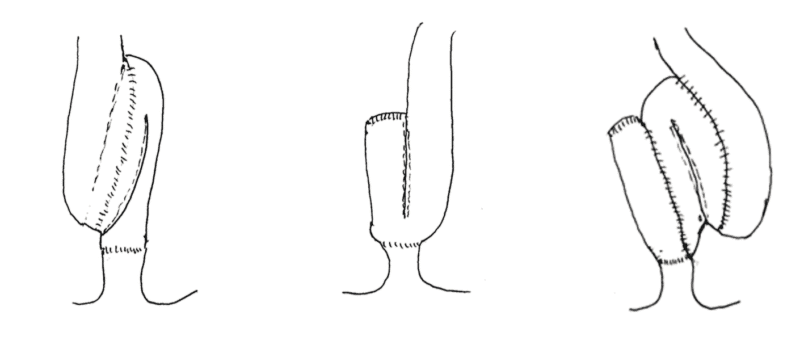
Allerede i 1933 beskrev professor Rudolf Nissen en kasuistikk med anleggelse av en dobbel ileumslynge i bekkenet med ileoanal anastomose hos en 12 år gammel gutt med familiær adenomatøs polyppose (1). Imidlertid tok det lang tid før reservoarideen ble gjenopptatt av Nils Kock i Göteborg, i form av en kontinent ileostomi (Figur 1), såkalt Kocks reservoar (2), som anses som forløperen til bekkenreservoaret. Det var først publikasjonen til Parks og Nicholls i 1978 som ble det virkelige startskuddet for bekkenreservoarkirurgien (3). I dette første pasientmaterialet, som besto av fem pasienter med ulcerøs kolitt, ble det konstruert et S-formet reservoar (figur 2a) med et 2-3 cm efferent løp som ble anastomosert til analkanalen på høyde med linea dentata. Bare en av de fem opererte pasientene oppnådde spontan tømming av reservoaret. Utsunomiya og medarbeidere publiserte to år senere de første resultatene etter anleggelse av et J-reservoar (figur 2b), som i tillegg til å være teknisk enklere å anlegge også ga pasientene mulighet til spontan tømming (4).
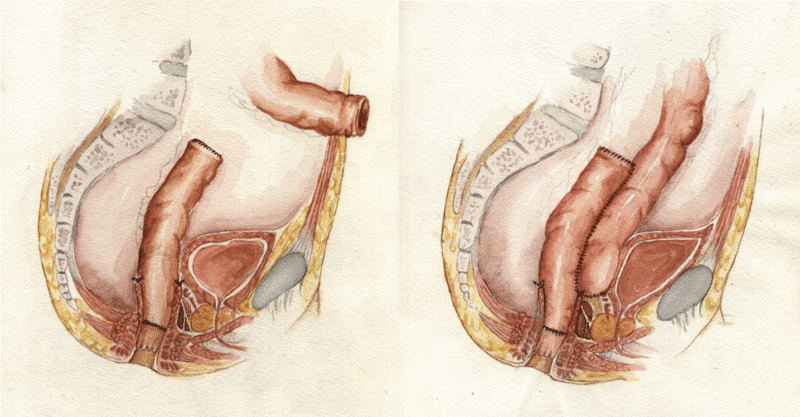
Det første bekkenreservoaret i Norge ble anlagt i Tromsø i 1980 av Gierckscy og Revhaug (5). I Tromsø brukte man initialt et såkalt lateralt ileumreservoar (Figur 3), der tilførende løp sys isoperistaltisk til fraførende løp (6). Man gikk imidlertid snart over til J-reservoar, som på grunn av dets enkelhet og relativt gode funksjon ble det mest valgte reservoaret både nasjonalt og internasjonalt. På 80- og 90-tallet ble det anlagt mellom 150 og 200 reservoarer årlig i Norge. Etter introduksjonen av biologisk behandling falt det årlige antallet anlagte reservoarer i Norge til om lag 50. På grunn av betydelig redusert volum ble det nedsatt en faggruppe i 2019, i regi av Norsk forening for kolorektalkirurgi (NFKK). Gruppen publiserte en rapport i 2021 hvor det ble anbefalt at reservoarkirurgien skulle sentraliseres til maksimalt fem sentre, og at fjerning av gammelt reservoar med samtidig anleggelse av nytt reservoar (redo) eller konstruksjon av kontinent ileostomi kun skulle gjøres ved én institusjon (7). Denne anbefalingen ble støttet av medlemmene i NFKK under høstmøtet i 2021.
Ulike reservoardesign
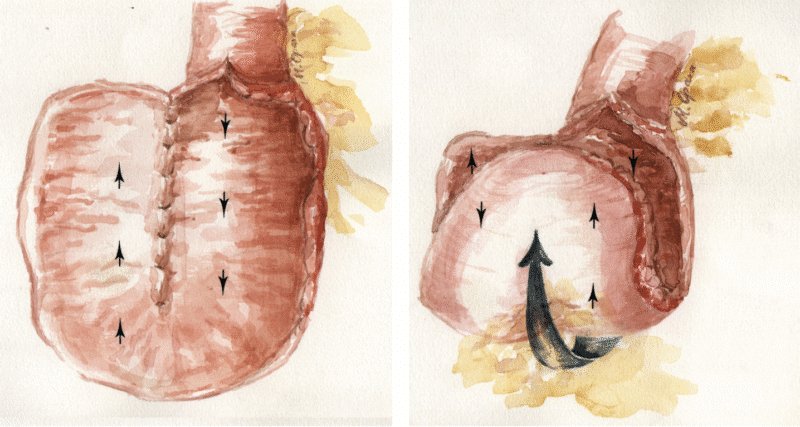
Initialt gikk man ut fra at større reservoar var forbundet med bedre kapasitet og dermed bedre funksjon. S-reservoaret, som initialt ble benyttet ved St Mark's Hospital i London, har tre slynger av ileum (Figur 2a), mens W-reservoaret benytter fire slynger (Figur 2c). Selv om S- og W-reservoar innebærer større reservoarkapasitet med behov for færre tømninger i døgnet, forsvinner denne fordelen over tid (8). I tillegg opplever flere pasienter med S- og W-reservoar tømningsvansker, noe som har bidratt til at J-reservoaret har befestet sin posisjon som den foretrukne konfigurasjonen (9). Ved Akershus Universitetssykehus (Ahus) har Øresland og kolleger over tid benyttet et såkalt K-reservoar, som innebærer at bakveggen sys som et J-reservoar, mens framveggen brettes fra distale slynge mot proksimalt slik at reservoaret blir kortere, men bredere enn et J-reservoar (Figur 4). Det er i en retrospektiv studie fra Ahus vist noe bedre reservoarkapasitet og funksjon med denne reservoarkonfigurasjonen sammenlignet med J-reservoar (10).
Indikasjoner og kontraindikasjoner
De to vanligste indikasjonene for proktokolektomi og anleggelse av bekkenreservoar er ulcerøs kolitt og familiær adenomatøs polypose (FAP). Bekkenreservoar kan også være en mulighet hos yngre pasienter med synkrone cancere i rektum og kolon.
Selv om det ikke finnes noen formell aldersgrense for når man skal avstå fra reservoaranleggelse, er det sjeldent at reservoar anlegges hos pasienter over 60 år (5). Hos kvinner må også eventuelt tidligere obstetrisk sfinkterskade sammenholdt med generelt dårligere sfinkterfunksjon postmenopausalt tas med i vurderingen. Videre kan overvekt medføre tekniske utfordringer med å få nok lengde på krøset til reservoaret, siden et fettholdig krøs blir kortere, og mange venter derfor med reservoarkirurgi til pasienten har en KMI <30. Dette er spesielt viktig hos høye pasienter, hvor kombinasjonen med kort krøs kan føre til at man ikke klarer å få nok lengde til å anastomosere.
Reservoarkirurgi er også en opsjon hos pasienter med udeterminert kolitt. På tross av mer effektiv medikamentell behandling vurderes fortsatt Crohns sykdom som relativ kontraindikasjon for reservoarkirurgi grunnet betydelig økt risiko for perianal fistelsykdom med behov for fjerning av reservoaret, blant annet tydeliggjort i en fersk publikasjon fra Cleveland Clinic, Ohio, med oppfølging av over 5000 pasienter med bekkenreservoar (11). Bekkenreservoar kan kun vurderes hos selekterte Crohnspasienter dersom det verken foreligger tynntarmsaffeksjon eller perianal sykdom. Pasientene med udeterminert kolitt eller Crohns sykdom må informeres godt om økt risiko for både komplikasjoner og reservoarsvikt.
Det er uansett viktig at pasienter som er aktuelle for bekkenreservoar informeres så nøkternt som mulig slik at de har realistiske forventninger. Selv om de fleste som tilbys anleggelse av bekkenreservoar velger denne løsningen, ønsker noen pasienter heller permanent ileostomi framfor å måtte gå på toalettet 5-7 ganger daglig. I utvalgte tilfeller der rektum ikke er affisert av kolitt kan også ileorektal anastomose være et alternativ til reservoar, men det praktiseres sjeldent for UC i Norge. Det er viktig at aktuelle pasienter henvises til sykehus som utfører reservoarkirurgi for å bli informert om de forskjellige alternativene. Vår oppgave som kirurger er å støtte pasientene i det valget de tar, og ikke prøve å overbevise dem til det ene eller andre.
Operasjon i en-, to- eller tre seanser?
Flertallet av pasienter med ulcerøs kolitt blir operert i tre seanser, der første seanse er kolektomi med endeileostomi. Når pasienten har kommet seg, gjerne 3-12 måneder etter kolektomien, utføres proktektomi med anleggelse av reservoar og bøyleileostomi, som legges tilbake i tredje seanse etter ca. 3 måneder. Hos pasienter som er i god allmenntilstand og ikke benytter steroider, men hvor det er operasjonsindikasjon på grunn av manglende symptomkontroll, dysplasi, FAP eller cancer, kan proktokolektomi med reservoaranleggelse gjøres i samme seanse. Det er vanlig i Norge å anlegge avlastende bøyleileostomi i forbindelse med reservoarkirurgi. I et materiale fra St. Olavs hospital, publisert av Wasmuth og medarbeidere, fikk 84 % av pasientene avlastende stomi (12). Stomi kan vurderes utelatt hos pasient med lav risiko for anastomoselekkasje, så som slank kvinne i god allmenntilstand, eller der hvor det ikke er mulig å få ut en god stomi på grunn av manglende lengde på krøset. Ved både Universitetssykehuset Nord-Norge (UNN) og Ahus anlegges avlastende stomi så sant det er teknisk mulig. Verken Wasmuth og medarbeider (12) eller Sahami og medarbeidere (13) fant at avlastende stomi var assosiert med lavere anastomoselekkasjerate, mens Plietz og medarbeidere i et materiale på 584 pasienter fant signifikant færre anastomoselekkasjer hos pasienter som hadde fått avlastende stomi (14).
Spesielle peroperative forhold
Proktektomi: Uansett om reservoaret anlegges i samme seanse som kolektomi eller etter at kolektomi er utført, er det de samme prinsippene som gjelder. Om det ikke er mistanke om malignitet kan proktektomien utføres tarmnært eller som en modifisert total mesorektal eksisjon (TME), der man bevarer en fettpute over promontoriet og holder seg tarmnært venterolateralt for å minimere risikoen for nerveskade. Rektum skal avsettes helt distalt, ca. 1-2 cm over linea dentata. Ved avsetning høyere opp øker risikoen for tømningsvansker, i tillegg til at ulcerøs kolitt i gjenværende rektumslimhinne, såkalt «cuffitt», kan skape problemer.
Preparering av terminale ileum: Noen anbefaler at arteria ileocolica bevares ved kolektomien, ettersom det gir mulighet for å øke rekkevidden av reservoaret ved å dele ileale kar, mens andre foretrekker alltid å dele de ileokoliske karene. Tynntarmskrøset til terminale ileum dissekeres så av bakre bukvegg så langt opp man kommer mot arteria og vena mesenterica superior (AMS og VMS). Dette gir vanligvis nok lengde til at reservoaret når tensjonsfritt ned til bekkenbunnen. Som en tommelfingerregel bør nederste punkt av reservoaret rekke minst 2 cm nedenfor nedre begrensing av symfysen. Dersom det er usikkert om lengden er tilstrekkelig kan man anlegge Z-insisjoner i peritoneum fra avgangen av AMS og videre distalt til terminale ileumslynge. Dette gir fort 2 cm ekstra lengde. Når det er avklart at krøset har tilstrekkelig lengde, anlegges reservoaret. Ved bruk av J-reservoar legges vanligvis krøset baktil, men ved utfordring med lengde kan krøset legges fortil, noe som kan gi ytterligere 1-2 cm lengde. Ved bruk av K-reservoar (Ahus) legges krøset alltid fortil. J-reservoar konstrueres ved å lage en åpning med diatermi i den slyngen av terminale ileum som gir mest lengde på krøset. Selve slyngen måles opp til ca. 15 cm, og reservoaret lages ved å benytte to GIA 80-magasin. Det er viktig å sjekke for blødning fra staplerradene på mukosasiden av reservoaret og at bakveggen er patent før hatten til sirkulær stapler sys inn. Ved K-reservoar syr man først bakveggen av to ileumslynger sammen på langs og syr in hatten til sirkulær stapler i enden av denne suturen før man syr framveggene sammen på tvers og snur reservoaret (Figur 4). Når reservoaret føres ned i bekkenet, er det viktig å påse at krøset ikke ligger rotert ved å følge krøskanten fra pankreas ned mot reservoaret, siden et torkvert krøs vil kunne gi både dårlig sirkulasjon og funksjonssvikt.
Anastomosen: Denne anlegges som regel transanalt med sirkulær stapler. Ved dysplasi i nedre rektum og ved FAP med polypper i distale rektum er det aktuelt med mukosektomi og håndsydd anastomose. En sjelden gang er det nødvendig med proktektomi hos barn som ikke er ferdig utvokst på grunn av behandlingsrefraktær betydelig proktitt, og da kan også håndsydd anastomose være eneste mulighet. Ved håndsydd anastomose må mukosa strippes av indre sfinkter fra linea dentata og ca. 1,5 cm mot proksimalt, slik at sfinkterfunksjonen ikke kompromitteres. Håndsydd anastomose er assosiert med noe dårligere funksjon i form av inkontinens og nattlig sekresjon og innebærer høyere risiko for reservoarsvikt over tid (11,15).
Til slutt anlegges en avlastende bøyleileostomi. Reservoaret skylles transanalt postoperativt for å hindre at det fyller seg med blod eller dilaterer og gir blow-out.
Åpen eller laparoskopisk teknikk
Det er ikke vist noen forskjell i reservoarfunksjon eller reservoarsvikt mellom de to teknikkene (16). Ved UNN og Ahus er laparoskopisk teknikk standard. Laparoskopi er noe mer tidkrevende enn åpen teknikk, men pasientene har de generelle fordelene ved laparoskopi postoperativt. Det synes imidlertid også som at laparoskopisk teknikk reduserer risikoen for manglende evne til spontan graviditet som er sett ved åpen teknikk (17,18). På grunn av nedsatt fekunditet er denne pasientgruppen uansett prioritert for IVF.
Resultater ved kirurgi for bekkenreservoar
Postoperative komplikasjoner: Som ved andre anastomoser i bekkenet forekommer også postoperativ anastomoselekkasje ved reservoaranleggelse, med rapportert lekkasjerate mellom 3 % og 20 % (11-14). Postoperativ bekkensepsis uten funn av anastomoselekkasje oppstår hos 3-4 % (11,12). I tillegg kan det ved J-reservoar lekke fra den blinde enden av reservoaret. Behandling av anastomoselekkasje følger vanlige prinsipper, inkludert mulighet for bruk av endokavitær vakuum-svamp med eventuell påfølgende transanal sekundærsutur av anastomosen (19).
Funksjon: Ca. 75 % av pasientene er fornøyde med reservoarfunksjonen i årene etter operasjon og over 95 % angir at de ville gjort operasjonen om igjen om de hadde fått valget på nytt (10). Et godt resultat innebærer 5-7 gjennomsnittlig tømninger i døgnet, og pasientene må forberedes på at de må påregne en nattlig tømning. Mange av pasientene vil være avhengig av avføringsmodulerende medikamenter som loperamid i perioder eller fast for å holde akseptabel tømningsfrekvens. Noen pasienter kan oppleve soiling eller mindre lekkasjer om natten, dette gjelder særlig ved håndsydd anastomose.
Senkomplikasjoner: I større materialer opplever over 50 % av pasientene en komplikasjon som krever kirurgisk behandling (12). De vanligste er fistulering, anastomosestriktur, bekkeninfeksjon, tømningsvansker og kronisk pouchitt med påfølgende dårlig reservoarfunksjon, som i noen tilfeller kan føre til utkobling eller fjerning av reservoaret (5,11). Det er uansett viktig å henvise disse pasientene til et senter som bedriver reservoarkirurgi, ettersom mange problemer kan håndteres uten utkobling av reservoaret. Kumulativ risiko for reservoarsvikt (definert som utkoblet eller fjernet reservoar) ved ulcerøs kolitt i større materialer er ikke mer enn ca. 9 % etter 20 år (5,11,12). Vi anbefaler at alle pasienter som har fått reservoar kontrolleres regelmessig for å kunne fange opp funksjonssvikt.
Alternativer til bekkenreservoar
Ileorektal anastomose: Ileorektal anastomose (IRA) har blitt brukt som et alternativ til bekkenreservoar i mange år. Fordelen med IRA er at det er et vesentlig enklere inngrep. Hovedproblemet med denne løsningen er at UC vanligvis er en ascenderende sykdom der sykdommen er verst i rektum. Kobler man tynntarm til endetarmen vil proktitten som regel residivere og ofte bli uhåndterlig. I dette tilfelle vil pasienter som ønsker en kontinent løsning måtte gjennomgå enda flere operasjoner for å ende opp med et bekkenreservoar. Samtidig kan IRA være en god (midlertidig) opsjon hos fertile kvinner med barneønske og for utvalgte pasienter med FAP hvis det er få eller ingen polypper i rektum (20). Man bør imidlertid ikke bruke denne løsningen hos pasienter med primær sklreoserende kolangitt (PSC)-relatert UC, selv om de ofte har en tilsynelatende frisk rektum. Grunnen til det er en vesentlig økt risiko for endetarmskreft hos pasienter med PSC og IRA (21).
Kocks reservoar (kontinent ileostomi): Kocks reservoar er en kontinent løsning som kan være et alternativ for pasienter der bekkenreservoar ikke er mulig eller hos pasienter som ikke ønsker bekkenreservoar. I dag er hovedindikasjonen for nytt Kocks reservoar først og fremst alvorlige hudproblemer ved ileostomi. Noen pasienter kommer imidlertid også med et ønske om Kocks reservoar fremfor et bekkenreservoar. Prinsippet for kontinent ileostomi er at man lager et ileumreservoar på innsiden av bukveggen med en ventilfunksjon konstruert av invertert tarm (Figur 1). Pasienten må da tømme reservoaret ca. fire ganger daglig ved hjelp av et kateter gjennom stomiåpningen i bukveggen. Fordelen med et velfungerende Kocks reservoar er at pasienten har full kontroll over tarmtømmingen. Ulempene er at ca. 50 % av disse pasienter har behov for reintervensjoner, hovedsakelig på grunn av sviktende ventilfunksjon, og at pasientene må holde en diett som sikrer at de får tømt avføringen gjennom kateteret. Kocks reservoar utføres etter 2021 kun ved Ahus, og aktuelle pasienter må gjerne henvises dit.
Konklusjon:
Bekkenreservoar er en etablert løsning hos pasienter med behandlingsrefraktær ulcerøs kolitt, samt ved enkelte andre tilstander. Kirurgien utføres ved fem universitetssykehus (Ahus, Haukeland, St. Olavs, Ullevål og UNN), mens kontinent ileostomi (Kocks reservoar) og eventuell reoperasjon med reanleggelse av nytt bekkenreservoar er anbefalt uført kun ved ett sykehus (Ahus). Selv om flesteparten av pasientene med bekkenreservoar er fornøyde med oppnådd funksjon, er reintervensjonsraten høy. Det er viktig at pasientene kjenner til alternativene ved kirurgi, og at pasienter som får anlagt reservoar følges regelmessig slik at komplikasjoner kan håndteres tidlig.
Referanser
- Nissen R. Demonstrationen aus der operativen Chirurgie, Nr. 39. In: Sitzungsberichte aus chirurgischen Gesellschaften. Berliner Gesellschaft fiir Chirurgie. Zentralbl Chir 1932; 60:88
- Kock NG. Intra-abdominal "reservoir" in patients with permanent ileostomy. Preliminary observations on a procedure resulting in fecal "continence" in five ileostomy patients. Ann Srg 1969; 99:223-231
- Parks AG, Nicholls RJ. Proctocoelctomy without ileostomy for ulcerative colitis. BMJ 1978; 2:85-88
- Utsunomiya J, Iwama T, Imajo M, et al. Total colectomy, mucosal proctectomy, and ileoanal anastomosis. Dis Colon Rectum 1980; 23:459-466
- Wasmuth HH. Ileal Pouches – Doctoral Thesis at NTNU. 2012:10 ISBN 978-82-471-3281-4 (electronic version)
- Fonkalsrud EW. Endorectal Ileal Pullthrough with Lateral Ileal Reservoir for Benign Colorectal Disease. Ann Surg 1981; 194:761-766
- https://kolorektal.no/wp-content/uploads/2024/11/Rapport-endelig-IBD-gruppe-v26.10.21.pdf
- McCormick PH, Guest GD, Clark AJ, et al. The ideal ileal-pouch design: a long-term randomized control trial of J- vs W-pouch construction. Dis Colon Rectum 2012; 55:1251-1257
- Lovegrove RE, Heriot AG, Constaninides V, et al. Meta-analysis of short-term and long-term outcomes of J, W and S ileal reservoirs for restorative proctocolectomy. Colorectal Dis 2007; 9:310-320
- Sunde ML, Øresland T, Færden AE. Restorative proctocolectomy with two different pouch designs: few complications with good function. Colorectal Disease 2017; 19:363-371
- Lavryk O, Maspero M, Holubar SD, et al. Postoperative outcomes of a pelvic pouch procedure: Lessons learned over 40 years among 5070 patients. J Gastrointest Surg. 2025; 29:101938. doi: 10.1016/j.gassur.2024.101938. Epub 2025 Jan 20.
- Wasmuth HH, Tranø G, Endreseth B, et al: Long-term surgical load in patients with ileal pouch-anal anastomosis. Colorectal Disease 2009; 11:711-718
- Sahami S, Buskens CJ, Fadok TY, et al. Defunctioning ileostomy is not associated with reduced leakage in proctocolectomy and ileal pouch anastomosis I surgeries for IBD, J Crhons Colitis 2016; 10:779-785
- Plietz MC, Kayal M, Rizvi A, et al. Slow and steady wins the race: a solid case for 3-stage approach in ulcerative colitis. Dis Colon Rectum 2021; 64:1511-1520
- Kirat HT, Remzi FH, Kiran RP, et al. Comparison of outcomes after hand-sewn versus stapled ileal-pouch-anal anastomosis in 3,109 patients. Surgery 2009; 146:723-729
- Mineccia M, Cravero F, Massucco P, et al. Laparoscopic vs open restorative proctocolectomy with IPAA for ulcerative colitis: Impact of surgical technique on creating a well functioning pouchInternational Journal of Surgery 2018; 55:201-206
- Bartels SA, DʼHoore A, Cuesta MA, et al. Significantly increased pregnancy rates after laparoscopic restorative proctocolectomy: a cross-sectional study. Ann Surg. 2012; 256:1045-1048
- Beyer-Berjot L, Maggiori L, Birnbaum D, et al. A total laparoscopic approach reduces the infertility rate after ileal pouch-anal anastomosis: a 2-center study. Ann Surg. 2013; 258:275-282
- Gradenbroek TJ, Musters GD, Buskens CJ, et al. Endo-sponge treatment of anastomotic leakage after ileo-anal pouch anastomosis: report of two cases. Colorectal Dis. 2015; 17:426-432
- Zaffaroni G, Mannucci A, Koskenvuo L, et al. Updated European guidelines for clinical management of familial adenomatous polyposis (FAP), MUTYH-associated polyposis (MAP), gastric adenocarcinoma, proximal polyposis of the stomach (GAPPS) and other rare adenomatous polyposis syndromes: a joint EHTG-ESCP revision. Br J Surg. 2024 May 3;111(5):znae070. doi: 10.1093/bjs/znae070
- M, Landerholm K, Andersson P, Andersson RE, et al. Risk of Rectal Cancer After Colectomy for Patients With Ulcerative Colitis: A National Cohort Study. Clin Gastroenterol Hepatol. 2017; 15:1055-1060